
Электронная книга - Бесплатно
Ничто не происходит без
достаточного основания.
М. В. Ломоносов, 1741 г.
Предисловие
Эта книга для людей инициативных, любознательных, склонных к творчеству и имеющих возможность выделить для своих занятий хотя бы немного свободного времени. Если следовать изложенным в ней советам и рекомендациям, то результат превзойдёт все ожидания и весьма благотворно скажется на здоровье, в том числе близких друзей и родственников.
Книга основана только на собственных материалах автора, полученных при изготовлении виноградной водки в домашних условиях.
Непосредственным поводом к началу работы и, как следствие, к написанию книги послужил банальный телевизионный сюжет «лихих» 90-х годов по пресечению милицией деятельности подпольных производителей спиртного. На телеэкране какой-то подозрительного вида субъект в телогрейке, не особо стараясь, разливал ковшиком по бутылкам замешенное в бытовой ванной пойло. В самом сюжете не было ничего особенного для того времени — грязь, тараканы, мухи, но поразительным было наличие внушительного количества новеньких, только что из печати фирменных этикеток известного отечественного изготовителя водки, которые вместе с акцизными марками наклеивались на бутылки с произведённым зельем. А тут ещё сосед по гаражному кооперативу угостил восхитительной померанцевой настойкой и под большим секретом сообщил, что вообще-то самостоятельно произведённый продукт (язык не поворачивается назвать его самогоном) это вовсе не та мутноватая жидкость, которую раньше в деревнях гнали из свёклы, разливали из чайника в 125 граммовые стаканчики и тут же накрывали их кружком свежего огурца — дух у напитка был весьма забористым (в далёком 1966 году автору — тогда ещё студенту «посчастливилось» попробовать такой самогон в стройотряде и воспоминания о нём не истёрлись из памяти до сих пор).
Известно, что домашнее производство крепких спиртных напитков в России существовало всегда. Кто-то занимался этим с целью наживы, а кто-то силу сложившихся обстоятельств. Например, далеко не бедный профессор Преображенский в «Собачьем сердце» М. Булгакова (1925 г.) весьма похвально отзывался о 40о водке, изготовленной его кухаркой — другой-то просто не было, так как продажа водки населению была запрещена ещё царским правительством после вступления России в Первую мировую войну в августе 1914 г. — весь этиловый спирт направлялся на нужды армии и медицины. Большевики в 1917 году продлили запрет и сняли его только в январе 1924 г. В массовую продажу водка поступила в октябре 1925 г. Крепость её составляла 30о.
То ли за специфическую реакцию на неё организма, то ли по имени инициатора её выпуска — председателя Совета народных комиссаров А. И. Рыкова в народе эту водку прозвали «рыковкой», хотя вплоть до 1940 года водку делали только из пшеницы, ржи, овса и ячменя. В 1926 г. в продаже появилась уже 40о водка, а в 1932 г. Сталин даже закрыл общества трезвости — нужны были деньги на индустриализацию страны [2].
Государство, держащее монополию на производство крепкого алкоголя, как могло, боролось с нелегальными производителями. Их штрафовали, отнимали оборудование, подвергали осмеянию в средствах массовой информации, привлекали к уголовной ответственности — на заре советской власти самогоноварение приравнивалось к контрреволюции и за него могли поставить к стенке, а по Указу Верховного Совета СССР от 1948 г. за изготовление и продажу самогона полагалось не менее 6 лет с конфискацией имущества.
Но что никогда и никем не ставилось под сомнение, так это относительная безвредность продукта. В зависимости от усердия и прилежности производителя самогон мог быть мягким и душистым или иметь грубый вкус и неприятный запах, но не было случая, чтобы кто-нибудь отправился к праотцам, выпив рюмку домашнего, да ещё настоянного на травах самогона. Изготовленный из натуральных продуктов, самогон, по существу, не был фальсифицированным алкоголем. Ведь никому и в голову не приходило писать на бутылке самогона «Коньяк» или «Водка». Само латинское слово falsifico означает подделку чего-либо в корыстных целях. Фальсификация — это когда в бутылке с этикеткой «Водка» содержится разведённый водой синтетический или гидролизный этиловый спирт, а то и сущая отрава — метиловый спирт. Например, в мае 2011 года российские туристы в Турции насмерть отравились фальсифицированным виски, содержащим метиловый спирт.
Массовая торговля именно фальсифицированными спиртными напитками, т.е. изготовленными не из пищевых и тем более не из зерновых продуктов, началась после того, как наш первый Гарант — Б.Н.Ельцин по какой-то одному ему известной причине, а скорее всего по пьяни, отменил успешно просуществовавшую более 68 лет государственную монополию на производство и реализацию крепких спиртных напитков. Эта монополия не только обеспечивала высочайшее качество отечественных водок и коньяков, но и приносила державе доход, достаточный для содержания вооружённых сил всего СССР (в 2010 г. в доходы государства попадало чуть более 1% от продажи спиртного). После отмены монополии Россия захлебнулась суррогатными напитками из гидролизного и синтетического спиртов, употреблявшихся в странах-изготовителях разве что для розжига мангалов и каминов. Отравления алкогольными суррогатами в конце 90-х годов стали широко распространённым явлением, и одному Богу известно, сколько десятков тысяч человек отправились на тот свет прямо с собственных именин или из-под новогодней ёлки. Только по официальным данным [4] в 1996 году от употребления алкогольных суррогатов в России погибло около 60 тыс. человек.
К 2006 году — времени начала работы над материалами книги, ситуация на рынке алкогольной продукции несколько нормализовалась — откровенная отрава практически исчезла. Но по данным СМИ в том же 2006 году в России было произведено 5 млрд. бутылок водки, из которых 50% были поддельными. А 18.06.2012 г. по телевизионному каналу ТВЦ прошло сообщение, что в 2011 году в РФ официально было произведено 940 млн. литров водки, акциз собран с 800 млн. литров, но в розничной торговле было продано аж 1 миллиард 530 миллионов литров, т.е. почти в полтора раза больше, чем выпустили официально. Понятно, что мелкие мошенники с ковшиками и ржавыми ваннами такого количества водки из ворованного спирта произвести не могли, да и столько стеклотары по помойкам не насобираешь. Это значит, что «левая» водка была произведена на тех же легальных спиртзаводах из неучтённого т.е. заведомо некондиционного сырья. Водкой из такого сырья не отравишься, но по вкусу она существенно хуже выпущенной официально. В том, что всё обстоит именно так, многие убеждались на собственном опыте, когда одна из двух купленных в магазине бутылок водки одной и той же марки, взятых с одной полки, на поверку оказывалась «палёной».
Дело в том, что повсеместное применение в производстве этилового спирта ректификационных колонн (о них см. ниже) позволило получать спирт высокой химической чистоты практически из любого сырья, хоть из коровьего навоза, что было наглядно продемонстрировано в прямом эфире корреспондентами телекомпании НТВ 15.10.2010 г. (правда, пить его они не стали). Мизерная себестоимость спирта, полученного ректификацией не из отборной пшеницы и ржи, а из чего угодно — гнилого картофеля, подопревшего зерна, мороженой свёклы, отходов сахарного, деревоперерабатывающего производства и химической промышленности, стала приносить фантастические доходы производителям, но водка из такого спирта перестала быть той водкой, какой она была даже до горбачёвской «перестройки». Во-первых, она утратила характерные аромат и послевкусие. Сейчас мало кто помнит, но ещё в 60-х годах прошлого века рюмку водки можно было с удовольствием выпить и не закусывая. Во-вторых, под воздействием выпитого, человек уже не расслаблялся и не приходил в благодушное состояние, а наоборот становился злым, нетерпимым и агрессивным. Последствия от употребления водки стали одинаково неприятными, независимо от того, какая водка была выпита накануне — за 200 руб. или за 1500 руб. — спирт ректификат в них один и тот же! Даже перегонять эту водку в домашних условиях с целью улучшения качества стало бессмысленным, т.к. любой кустарный перегонный аппарат не может сравниться по точности разделения спиртосодержащих смесей с промышленной ректификационной колонной, и дело вовсе не в точности перегонки, а в природе используемых для брожения продуктов. Если для производства водки используются кондиционная пшеница, рожь, ячмень, свежий виноградный жом или, наконец, обыкновенный сахар, то для получения качественного продукта вполне достаточно всего двух перегонок виноматериала на дистилляторе заурядной конструкции. Если же исходные продукты были некачественными, то сколько спирт не перегоняй хоть в дистилляторе, хоть в ректификационной колонне, в какие красивые бутылки не разливай — водка из него от этого лучше не станет. И абсолютно не имеет значения, отвечал ли формально исходный пищевой спирт требованием одного из четырёх существующих на него ГОСТов: «Люкс», «Экстра», «Высшей очистки», «1-го сорта». Всё определяется самочувствием на следующий день после употребления спиртного, даже если накануне водка или коньяк были вполне приемлемыми на вкус. Человеческая алчность пределов не имеет, и проходимцы тоже совершенствуют своё мастерство, к тому же достижения современной химии позволяют фальсифицировать вкус и запах чего угодно.
Насколько успешной может быть такая фальсификация хорошо видно из следующего примера. Как-то в мае 2012 г. телевидение пригласило группу добровольцев человек из двенадцати, самому старшему из которых на вид было лет 40 с небольшим, для дегустации коньяков в прямом эфире. Дегустаторам (это слово надо бы взять в кавычки) предварительно завязали глаза, а затем дали попробовать три сорта налитого в рюмки коньяка для определения лучшего по качеству. Ребята старательно прихлёбывали и причмокивали, что-то там говорили насчёт букета, аромата и терпкости, но в итоге оконфузились практически все. Когда им сняли повязки, в двух из трёх рюмок оказалась жидкость синего и зелёного цвета, ничего общего не имеющая с коньяком, а в третьей дешёвенький коньяк сомнительного производства. Да и откуда им знать, что такое настоящий коньяк, если самый старший из них родился через 20 лет после того, как настоящий коньяк перестали выпускать (по крайней мере, для широкой продажи). Ну не производит Россия такого количества винограда, чтобы коньяком из него можно было торговать на каждом углу, да ещё по 350 руб. за бутылку.
Но использование недоброкачественных, хотя и пищевых продуктов при производстве этилового спирта — это ещё не вся беда! В технике в громадных количествах получают синтетический этиловый спирт прямой гидратацией этилена [5]. И не иначе как под нажимом водочной мафии, «высокоочищенный» синтетический спирт недавно прошёл токсикологическую экспертизу и разрешён Госсанэпиднадзором РФ для использования в качестве сырья в пищевой промышленности и в производстве алкогольных напитков [6]. И дело не в том, что в России с зерном и картошкой плохо. Просто синтетический этиловый спирт в 6 раз дешевле пищевого — вот и вся арифметика. Кто не верит, пусть обратит внимание на то, как по всей России один за другим разоряются спиртзаводы, производившие водку из натуральных пищевых продуктов по традиционной технологии. А раз так, то синтетический спирт будут непременно добавлять в водку и вопрос только в какой пропорции с «пищевым». Если как в анекдоте про пирожок с рябчиком, в котором половина лошади и половина рябчика, то тогда понятно, почему столько водки производится в некоторых республиках РФ, в которых посевных площадей под пшеницу или картофель практически и нет.
В общем, сложилось положение, выйти из которого можно было двумя путями: или навсегда лишить себя удовольствия согреться с морозца рюмкой рябиновой или анисовой настойки, или научиться получать пищевой этиловый спирт самостоятельно, тем более что его изготовление для собственных нужд законом не запрещено. К тому же опутавший дачный забор виноград широко распространённого сорта Изабелла, из которого при определённых навыках получалось неплохое вино, представлял собой превосходный источник практически дармового сырья.
Обращение к наводнившей в то время книжный рынок литературе по домашнему изготовлению водок сразу же выявило тот факт, что авторы этих изданий (иногда их фамилии даже отсутствовали в выходных данных на книгу) сами никогда перегонкой не занимались. Предлагаемые ими конструкции самогонных аппаратов были ненадёжны, взрывоопасны и, как правило, перерисованы с какого-то одного и того же древнего источника, когда в ходу были печные чугунки. Наоборот, в Интернете рекламировались (в основном на продажу) вполне профессионально сконструированные и изготовленные дистилляторы, но общим их недостатком, наряду с ценой в несколько десятков, а то и сотен тысяч рублей, были вес в незаполненном виде (до 50 кг.) и габарит (высота собранной ректификационной колонки 1,5–1,9 м.). Последнее существенно затрудняло возможность использования таких аппаратов в условиях городской квартиры, т.е. проведения перегонки на обычной газовой плите высотой около 0,9 м при типовой высоте потолков 2,65 м. Кроме того, для изготовления качественного продукта совершенно не требуется высокая степень химической чистоты получаемого спирта — иначе водка из него потеряет характерный аромат и послевкусие, и станет той водкой, которую сейчас продают в магазинах, т.е. в разбавленный водой химический реактив «Спирт этиловый», крайне вредный для здоровья (о чём будет сказано ниже).
Встречались и совсем уж экзотические предложения. Так в №2 еженедельника «АиФ» в январе 1999 г. рекламировался домашний автоматический микроспиртзавод по габаритам меньше телевизора, якобы позволяющий производить из 1 кг. сахара аж целых 6 бутылок высококачественной водки. Это ни что иное как откровенная дезинформация, поскольку подсчёт молярных масс по обе стороны уравнения распада глюкозы на этиловый спирт и углекислый газ (см. ниже) с учётом плотности спирта 0,8 кг∕литр даёт выход спирта из 1 кг. глюкозы не более 0,64 л., из которых при разбавлении до 40о получается всего 1,08 литра водки [7].
Поскольку ставилась задача создать, так сказать «семейный» аппарат, т.е. небольшой по объёму, разумный по весу, быстро входящий в рабочий режим, достаточно производительный и автоматизированный ровно настолько, чтобы за ним не требовалось постоянного наблюдения, то пришлось обратиться к профессиональной литературе — учебникам по органической химии, справочникам, пособиям по проведению лабораторных работ и т. п.
В результате удалось спроектировать и изготовить компактный, высокопроизводительный и абсолютно безопасный в работе перегонный аппарат, позволяющий в домашних условиях получать этиловый спирт высокого качества, как из перебродившего виноградного сока, так и других спиртосодержащих жидкостей натурального происхождения.
Конструкция этого аппарата, а также различные технологические приёмы сбраживания, перегонки, очистки и настаивания полученного продукта, опробованные автором, предлагаются вниманию читателей вместе с рассмотрением сопутствующих физических и химических явлений, важных для понимания и правильного проведения процесса перегонки.
Автор благодарен Анатолию Павловичу Шулаеву, организовавшему изготовление аппарата в условиях разваливающегося промышленного производства, Виктору Алексеевичу Ульянову — за предоставление первоначальной рецептуры получения виноградного вина, Виктору Георгиевичу Ворожейкину — за помощь в изготовлении ректификационной колонки и хроматографические исследования качества отдельных фракций при дробной перегонке в лаборатории ЗАО «Тест–3», а также директору этой организации академику РАН Звереву Юрию Ермолаевичу, благосклонно закрывавшему глаза на нецелевое использование дефицитных расходных материалов, необходимых для этих исследований.
Автор также весьма признателен Киму Павловичу Дробышеву — упомянутому выше соседу по ГСК за посвящение в секреты мастерства, кандидату химических наук Максиму Валериевичу Кузнецову за ряд ценных замечаний по материалам книги и предоставление специальной литературы, Владимиру Викторовичу Мезину за разработку электронной схемы сигнального устройства, а также Ольге Фёдоровне Казмичёвой, любезно взявшей на себя труд по редактированию и вёрстке книги.
Отдельное спасибо дочери и зятю автора — Елене Михайловне и Андрею Викторовичу Новиковым за оформление книги и издание пробных экземпляров, а также сыну — Андрею Михайловичу, проявившему незаурядное терпение при поиске и ксерокопировании нужных автору материалов.
Глава 1. Немного истории
Приготовление вина путём сбраживания виноградного сока было известно ещё в доисторические времена [8]. Древним египтянам и германцам было знакомо пивоварение, а у северных народов уже довольно рано изготавливались спиртные напитки из мёда. Однако получение винного спирта путём дистилляции виноградного вина стало известно значительно позже. Это открытие было сделано, по-видимому, в XI столетии, вероятнее всего в Италии, хотя сам процесс дистилляции был известен почти за тысячелетие до нашей эры [9]. Так ещё в трудах Аристотеля (384–320 гг. до нашей эры) содержится указание как испарять воду нагреванием и сгущать образовавшиеся пары охлаждением, а Зосим во II столетии нашей эры описывает дистилляцию, как уже давно известный процесс. Но получение именно винного спирта путём дистилляции вина и конденсации паров в змеевиковом холодильнике впервые описано итальянцами Марком Греком и Таддеусом Флорентином около 1250 г. [8]. Полученное вещество оказалось прозрачной, легко воспламеняющейся жидкостью, обладающей более сильными по сравнению с вином опьяняющими свойствами, из-за чего было названо по-латыни «спиритус вини» — дух вина. Отсюда произошло старинное русское название спиритус, трансформировавшееся позднее в спирт.
В ХIII веке винный спирт применяли только в качестве лечебного средства — в начале секретного. Известный философ и теолог Лулл (1235–1315 гг.) восхвалял способность винного спирта «превращать стариков в юношей» и, ввиду особой ценности вещества, рекомендовал хранить его только в золотой посуде. Кроме того, спирт играл определённую роль в алхимических опытах над получением золота и, особенно, «камня мудрецов» и «жизненного» эликсира. Позднее из-за высокой способности спирта растворять различные вещества его стали использовать в качестве растворителя при изготовлении настоек и эссенций. Распространению винного спирта за пределами Италии как лекарственного вещества в значительной мере способствовала эпидемия чумы в 1348 г. В начале ХVIII века в качестве лечебного средства вошла в употребление смесь винного спирта с его эфиром под названием капель Гофмана (2 части 90% спирта и 1 часть серного эфира).
Арабское название алкоголь, под которым понимали любой мелкодисперсный порошок, было впервые дано чистому винному спирту Парацельсом (1493–1541гг.) в XVI веке.
Вопрос о составе и строении винного спирта горячо дискутировался в XVII и XVIII веках. На основе господствовавших в то время взглядов Сталь (1697 г.) считал его соединением тонкой кислоты с растительным маслом и водой [8]. По Боергаву (1732 г.) он являлся носителем горючести всей материи — простым невесомым веществом с названием флогистон. Картейзер (1736 г.) утверждал, что виноградный спирт это соединение чистого флогистона с чистым водным элементом.
В Россию виноградный спирт был впервые завезён генуэзским посольством, следовавшим через Московское княжество из Кафы (Феодосия) в Литву по случаю обращения литовского народа в католичество [10]. Под названием аквавита (aqua vitae) он был продемонстрирован княжескому двору, но был признан очень крепким и возможным для употребления только в разбавленном водой виде в исключительно медицинских целях. Второй раз аквавита была завезена в Россию в большем количестве в 1429 г. и снова генуэзцами [9]. Следуя в Литву на Тракайский съезд, на котором великому князю Литвы Витовту должен был быть присуждён королевский сан, они подарили Василию III Тёмному аквавиту в качестве лекарства, но на этот раз напиток был признан не только вредным, но и ввоз его в Московское государство был запрещён.
Начало производства винного спирта из зерновых продуктов в Московском государстве относят к периоду 1425–1440 г., поскольку уже не позднее 1478 г. Иоанн III ввёл государственную монополию на винокурение [9], а в 1506 г. шведский историк сообщал о вывозе из Москвы особого напитка под названием «горящего вина» [2]. Однако вопрос о том, что же послужило первоначальным толчком к началу производства пьянящего напитка в России и именно из зерна, в литературе не освещается.
Известно, что все свои знания человек, так или иначе, получил путём наблюдения и осмысления различных явлений в природе, которые имели место в ходе его хозяйственной деятельности, когда результат мог быть сознательно воспроизведён какое угодно количество раз подряд. Так естественный процесс образования капель росы на поверхности почвы и наземных объектах при понижении температуры воздуха в предутренние часы, а также закрепившиеся в языке вкусовые качества воды в этих каплях, были известны человеку, наверное, ещё до того, как он научился говорить. Но процесс дистилляции был открыт после того, как наблюдательный доисторический повар впервые накрыл холодной крышкой кипящую жидкость и обнаружил, что на вкус капли жидкости на крышке отличаются от вкуса жидкости в котле (скорее всего, почувствовал отсутствие в них соли).
Точно также при изготовлении и хранении виноградного сока первоначально случайно было установлено, что в неплотно закрытом сосуде он скисает и приобретает пьянящие свойства. Целенаправленное воспроизведение и совершенствование этого процесса позволило получить виноградное вино, а при нагревании вина до температур близких к кипению в каплях конденсата на крышке сосуда был обнаружен винный спирт. После этого дистилляция виноградного вина с целью получения качественного виноградного спирта была лишь вопросом времени. Таким образом, винный спирт был обнаружен и получен в Европе в результате анализа ряда довольно простых явлений, таких как широко распространённое естественное сбраживание виноградного сока в вино и его перегонка в спирт путём дистилляции.
Но, с другой стороны, хорошо известно [11], что получение спирта из зерновых культур является значительно более сложным процессом. Для этого необходимо наличие в одном месте солода — обычно это ячмень, проросший в затемнённом помещении ростками длиной до 1,0–1,5 см.; увлажнённых зёрен пшеницы или ржи, содержащих крахмал; дрожжей, вызывающих спиртовое брожение осахаренного солодом крахмала зерна, а также перепада температур: от 15–17оС, необходимых для протекания процесса брожения, до 9–10оС, при которых происходит конденсация спиртосодержащих водяных паров. Разумеется, что и само зерно должно быть в некотором избытке, чтобы хлебороб не обращал внимания на непригодность для хлебопечения его незначительной части. В этом смысле представляется интересной и не лишённой основания версия о происхождении водки в России, высказанная технологом одного из ликёроводочных заводов в передаче Российского радио 14.09.1999 г. Она, в частности, утверждала, что возможность получения пьянящих жидкостей из зерновых продуктов была обнаружена древними славянами после того, как из-за избытка зерна у них стало привычным хранить его в крытых ямах. Действительно во второй половине XV века — времени, к которому относят появление в России винокурения из ржи и пшеницы, сельское хозяйство в Московском государстве перешло на прогрессивную трёхпольную систему земледелия, что резко увеличило урожайность зерновых культур и способствовало появлению излишков хлеба [10]. При хранении зерна в ямах просачивающаяся сквозь перекрытия влага, в конечном счёте, приводила к его сбраживанию с выделением тепла и образованием спиртосодержащих паров. Пары, в свою очередь, конденсировались в капли на холодных деталях конструкции перекрытия ямы. Кому-то первому пришло в голову их лизнуть (не отсюда ли выражение «нализаться»? ), что и привело к обнаружению пьянящих свойств.
По сообщению того же технолога первоначально существовало три способа получения зерновой водки. По первому способу зерно заливалось водой в корчаге — развалистом глиняном сосуде с очень широким горлом и выдерживалось в тёплом месте до окончании брожения, которое протекало под действием диких дрожжей, всегда находящихся на поверхности зёрен и вызывающих иногда самовозгорание зерна при небрежном хранении. Затем горло корчаги закрывали овечьей шкурой (шерстью внутрь) и под её край бросали в корчагу раскалённые на огне камни. Содержимое в корчаге закипало и интенсивно испарялось, а спиртосодержащий водяной пар конденсировался на шерсти шкуры. Её отжимали и получали жидкость с известными свойствами. По второму способу на горло корчаги с перебродившим зерном натягивали мочевой пузырь быка. Водяной пар проходил сквозь стенку пузыря, а спирт, имеющий сравнительно больший размер молекулы, задерживался на внутренней поверхности пузыря, конденсировался и капал обратно в корчагу. В результате его концентрация в исходном продукте увеличивалась. Третий способ заключался в вымораживании — вынесении процеженной спиртосодержащей смеси на мороз. При этом часть воды в ней превращалась в лёд, а незамёрзший остаток обогащался спиртом.
История распространения винокурения на Руси, последствия введения и отмены государственных монополий на производство водки подробно описаны в целом ряде работ, из которых наиболее известной является упомянутая выше книга Вильяма Васильевича Похлёбкина «История водки» [10]. Однако, относиться к ней нужно с достаточной осторожностью, поскольку книга содержит ряд, мягко говоря, неточностей. Например, описание технологического приёма улучшения качества воды путём насыщения её жидким кислородом, уменьшение веса смеси при разведении этилового спирта с водой и обстоятельное, порой излишне эмоциональное, изложение расхожей байки о Дмитрии Ивановиче Менделееве как о создателе русской (московской) «монопольной» водки, хотя в его докторской диссертации «О соединении спирта с водою» [12] о водке нет ни слова. Правда, водка сыграла роковую роль в судьбе последнего прямого потомка Д. И. Менделеева — некоего Каменского А. Е., безвременно умершего по сообщению телекомпании НТВ 22.03.2008 года.
Из приведённого краткого исторического обзора следует, что для успешного изготовления водки в домашних условиях, в том числе и виноградной, а также для грамотного проектирования перегонного аппарата необходимо иметь представление о процессах брожения, испарения, кипения, дистилляции, а также обладать знаниями о физических и химических свойствах получающихся в результате брожения продуктов.
Начнём с брожения.
Глава 2. Брожение
Брожение (ферментация) — являлось наиболее изученным в прошлые времена химическим явлением.
Опытным путём было выяснено, что спирт образуется в результате брожения лишь сладких (содержащих сахар) веществ, что в процессе брожения образуется газ, признанный позже фиксированным воздухом, и характерный осадок на дне сосуда. Однако брожение первоначально рассматривали как процесс разложения, вызванный веществом, которое само находится в стадии разложения. В 1659 г. существовала такая теория брожения [8]: «Ферментация — это внутреннее движение, которым охвачены с помощью необходимой для этого влажности, различные, не слишком связанные между собой составы (из соли, масла и земли), которые благодаря длительному перемещению относительно друг друга, взаимно сталкиваются и истираются. В результате этого нарушается существовавшая взаимная связь частиц и оторвавшиеся частицы, уменьшившиеся в размерах благодаря постоянному трению, переводятся в новое, более прочное соединение».
Химический процесс спиртового брожения был впервые разъяснён Антуаном Лаувазье [16] в 1789 г. Путём количественных исследований он показал, что сахар распадается при брожении на этиловый спирт и углекислоту (по Лаувазье при этом также образуется и уксусная кислота).
В 1836 г. французский учёный Шарль Каньяр де Ла-Тур установил, что спиртовое брожение неотъемлемо связано с ростом и размножением дрожжей [16]. Бродильная сила дрожжей первоначально объяснялась двумя принципиально различными предположениями. Луи Пастер в 1857 г. пришёл к выводу, что спиртовое брожение могут вызывать только живые дрожжи в анаэробных (без кислорода) условиях [17]. Своё предположение он основывал на том, что стерилизованные растворы сахара, если их предохранить от попадания дрожжевых зародышей из воздуха, не подвергаются брожению. Тем самым было доказано, что спиртовое брожение вызывается дрожжами, и поэтому долгое время считали, что процесс расщепления сахара на спирт и углекислый газ обязательно связан с жизнедеятельностью дрожжей.
В противовес этому немецкий учёный Юстус Либих (1803—1873 г.г.) настаивал на том, что разложение сахара представляет собой явление, лишь сопутствующее росту дрожжей, но не является частью собственно жизненных процессов этих микроорганизмов. Однако теория Либиха в то время не получила широкого распространения. Общепринятое предположение Пастера о том, что брожение могут вызывать только живые дрожжи, было опровергнуто в 1871 г. русским врачом-биохимиком М. М. Манассеиной, установившей путём ряда опытов, что и совершенно убитые дрожжевые клетки способны вызывать брожение [5]. Через 26 лет в 1897 г. немецкий биохимик Бухнер повторил её опыты и подтвердил, что брожение не требует обязательного присутствия именно живой клетки. Для этого он уничтожил клеточные оболочки дрожжей, растерев их с кварцевым песком. Из полученной массы он под большим давлением выжал сок и установил, что ничтожная добавка этого сока вызывает брожение большого количества сахара. Чтобы опровергнуть утверждение оппонентов, что брожение вызывается находящейся в отжатом соке «живой протоплазмой», Бухнер предварительно убил дрожжи ацетоном, а затем показал, что сок, отжатый из таких дрожжей, не уступает по действию соку, отжатому из живых клеток [18]. Попутно было установлено, что при нагревании до 50оС и выше сок в обоих случаях утрачивает бродильные свойства.
Таким образом было доказано, что брожение вызывается находящимся внутри дрожжевых клеток веществом, которое не теряет своей активности и вне дрожжевой клетки. Это вещество, вызывающее спиртовое брожение, Бухнер назвал зимазой. Оно относится к группе веществ, называемых энзимами или ферментами (см. выше).
Превращение сахара в спирт и углекислый газ происходит при контакте с ферментом, т.е. внутри дрожжевой клетки. Выделяемый клеткой спирт равномерно и неограниченно растворяется в бродящей жидкости, но углекислый газ имеет предел растворимости. Поэтому по достижении насыщения он начинает скапливаться на поверхности дрожжевых грибков. В результате они всплывают к поверхности (визуально жидкость как бы кипит), где газ освобождается, а дрожжи опускаются на дно сосуда.
В 1905 г. русский химик Л. А. Иванов обнаружил, что добавление фосфатов в несколько раз повышает скорость брожения. В ходе дальнейшего изучения механизма спиртового брожения, в основном русскими и немецкими учёными было установлено, что часть энергии, освобождающейся при расщеплении сахара, запасается дрожжевыми клетками в виде АТФ (микроскопических, богатых энергией фосфатных соединений), что обеспечивает дрожжам их разнообразные энергетические потребности. В аэробных (в присутствии кислорода) условиях жизнедеятельности дрожжи разлагают сахара полностью до воды и углекислого газа с выделением определённого количества тепловой энергии. При анаэробных (в отсутствии кислорода) условиях дрожжи не доводят расщепление сахаров до конца и в процессе их жизнедеятельности образуется этиловый спирт и углекислый газ. Но выделяемое при этом количество теплоты составляет примерно 7% от энергии, выделяющейся при полном распаде сахаров до воды и углекислого газа. Компенсируя этот недостаток, дрожжи вызывают усиленное брожение. При наличии кислорода спиртовое брожение угнетается или прекращается совсем. В этом случае дрожжи получают энергию для жизнедеятельности в процессе дыхания и, при достаточном количестве пищи, содержащей азот и фосфор, усиленно размножаются, не вызывая спиртового брожения.
При техническом спиртовом брожении, когда в качестве сырья используется предварительно осахаренный солодом крахмал зерновых культур или картофеля, дополнительно образуются так называемые сивушные масла, открытые Кагуром в 1839 г. Сивушные масла представляют собой смесь летучих высших спиртов — н-пропилового, изопропилового, изобутилового, двух амиловых, гексилового и гептилового. Кроме того, получается некоторое количество янтарной кислоты [17]. Эти побочные продукты образуются из аминокислот белковых веществ, содержащихся как в исходных материалах для винокурения, так и в меньшей степени в белках собственно дрожжевых клеток, количество которых непрерывно пополняется вследствие процессов белкового обмена у дрожжей. Продукты расщепления этих белковых веществ доставляют усвояемый азот, необходимый для жизнедеятельности дрожжей, и при этом переходят в соответствующие альдегиды, а затем и в высшие спирты. Поэтому количество образующихся в бродильной жидкости сивушных масел можно существенно уменьшить, если усвояемый азот давать дрожжам в виде аммониевых солей, например, сернокислого аммония. Если же к бродильной жидкости прибавить лицин, то выход сивушного масла увеличится [17].
Из сказанного следует ещё один важный вывод. Несмотря на то, что в сбраживаемом виноградном соке отсутствуют растительные белки, а азотистых веществ вполне достаточно для обеспечения жизнедеятельности дрожжей, тем не менее, при перегонке такого виноматериала возможно наличие в дистилляте некоторого количества сивушных масел, образующихся при расщеплении белков самих дрожжевых грибков. Однако количество сивушных масел при брожении виноградного сока (или сахарной браги) будет, естественно, существенно меньшим, чем при перегонке браги, из зерна, сахарной свёклы и, тем более, из картофеля.
Кроме спиртового брожения, в результате которого образуется этиловый (винный) спирт, существуют и другие виды брожения, широко используемые в хозяйственной деятельности человека [16]. К ним относятся:
Молочнокислое брожение, которое вызывается двумя группами грибков. Первые в процессе брожения расщепляют моносахариды — глюкозу и фруктозу с образованием молочной кислоты. Вторые — ведут сбраживание с образованием молочной кислоты, уксусной кислоты, этилового спирта, углекислого газа и некоторого количества ароматических веществ. Соответственно, в первом случае молочнокислое брожение используется для получения молочной кислоты при изготовлении различных кисломолочных продуктов и для силосования кормов в сельском хозяйстве. Во втором случае брожение происходит при консервировании различных плодов и овощей путём квашения.
Уксусное брожение, которому подвержены спиртосодержащие жидкости. Оно заключается в окислении этилового спирта в уксусную кислоту особыми бактериями, называемыми уксусными грибками. Эти бактерии, размножаясь на поверхности содержащих спирт жидкостей, окисляют этиловый спирт кислородом воздуха в уксусную кислоту. Так как бактериям нужна пища, содержащая, как было отмечено выше, азот и фосфор, то уксусное брожение может происходить в виноградном соке, вине и пиве. В водных растворах чистого спирта, не содержащих соединений азота и фосфора, уксусное брожение не происходит.
Очевидно, что в окружающей среде все упомянутые дрожжевые грибки находятся не только повсеместно и одновременно, но и в некотором избытке. В самом деле, ни одной домохозяйке и в голову не придёт искать где-то молочнокислые бактерии для квашения капусты или засолки огурцов. Все ингредиенты просто закладываются в подходящую тару, заливаются (при солении огурцов или томатов) тёплой водой, а сверху помещают небольшой груз, чтобы плоды находились под слоем рассола [20]. Горло сосуда обвязывают салфеткой и, как любил говорить один обанкротившийся политик, «процесс пошёл».
Ещё более интересным, с этой точки зрения, представляется процесс изготовления в домашних условиях яблочного уксуса [21]. Здесь его уместно рассмотреть, чтобы не допустить скисания в уксус виноградного сусла при брожении.
Для получения яблочного уксуса готовится кашица из перетёртых сладких яблок, желательно осенних сортов созревания, в которых больше полезного полисахарида пектина. В неё для увеличения крепости конечного продукта добавляется сахар и некоторое количество воды для образования жидкой субстанции. Туда же вносится 1—2 ломтика подсушенного ржаного хлеба без подгорелых корок — источника витаминов группы В и немного пекарных дрожжей или бродящего виноградного вина, содержащего дрожжи. Горло сосуда (по возможности широкое для свободного доступа кислорода) обвязывается марлей с крупной ячеёй, чтобы в него не попадал случайный мусор. а сам сосуд помещается в тёплое затемнённое место. В сосуде одновременно протекают два процесса. Сначала вызывающие спиртовое брожение дрожжи сбраживают сахар и яблочный сок в этиловый спирт, а затем уксусные грибки окисляют спирт кислородом воздуха в уксусную кислоту. При правильном выборе соотношения участвующих в брожении ингредиентов яблочный уксус получается достаточно крепким независимо от того, где его делали — в Москве или в Хабаровске. Важно, чтобы дело происходило в тёплое время года, а яблоки были из местных садов, а не импортными, которые даже черви не едят.
Из сказанного можно сделать ряд практических выводов:
— Для увеличения выхода спирта заготовку предназначенного для изготовления вина и водки винограда нужно проводить в то время, когда гроздья наберут наибольшую сахаристость, т.е. в средней полосе России со сбором урожая можно не спешить до конца сентября.
— Если брожение будет производиться на «диких» природных дрожжах, находящихся на самом винограде, то сбору урожая должны предшествовать несколько сухих и тёплых дней — дожди смывают дрожжевые грибки с поверхности ягод.
— Во избежание уксусного скисания, переработка винограда в мезгу — смесь раздробленных ягод винограда и гребней, должна начинаться в течение нескольких часов после сбора винограда. Следует избегать попадания в мезгу ягод, расклёванных птицами — мало ли чего есть в их слюне.
— Брожение сусла — отжатого виноградного сока с добавленными в него сахаром (для увеличения выхода спирта) и водой (для уменьшения кислотности, если сок забраживается на вино) должно производиться в анаэробных условиях, т.е. без доступа кислорода воздуха.
— Недопустимо использование при брожении алюминиевой тары, особенно когда сок забраживается для получения виноградного вина. Дело в том, что присутствующая в бродильной жидкости уксусная кислота взаимодействует с алюминием с образованием растворимых в воде уксуснокислых солей алюминия [5]. Ничего хорошего от их попадания внутрь организма не будет, т.к., например, уксуснокислый алюминий является часто применяемым антисептиком, а в промышленности он используется в качестве протравы для текстильных волокон.
Всё сказанное выше относилось к процессам брожения, протекающим при непосредственном участии дрожжей. Что же представляют собой дрожжи и подвергаемые ими брожению продукты?
Глава 3. Дрожжи и углеводы
Дрожжи ниспосланы человеку Создателем не иначе как в подарок. Произошло это, по-видимому, на пятый или шестой день Творения [23], когда у него дошли руки до сотворения всего живого, поскольку дрожжи относятся к микроорганизмам — обширной группе живых, преимущественно одноклеточных существ [19]. Микроорганизмы вездесущи и неистребимы. В 1 грамме почвы их содержится до 2–3 млрд. Они встречаются в атмосфере на высоте 20 км. над землёй и в мировом океане на глубине 11 км, в Арктике, в Антарктике и песках пустыни. Определённое их количество всегда присутствует в слюне, они также непосредственно участвуют в пищеварительном процессе в кишечнике, где их по некоторым данным содержится до трёхсот разновидностей общим весом 3—4 кг.
Микроорганизмы-дрожжи, вызывающие спиртовое брожение сахаристых веществ, носят название сахаромицетов и относятся к семейству сумчатых одноклеточных грибов. В природе их насчитывается 2 тысячи родов и 15 тысяч видов [19]. Всё тело этих грибов состоит из одного микроскопического пузырька-клеточки округлой, яйцевидной или овальной формы размером 5–7 мкм в ширину и 8–11 мкм в длину [16].
Как и у всего живого у них, естественно, имеет место половой процесс, который заключается в том, что обычно две внешне одинаковые, реже различные клетки сближаются и сливаются вместе — копулируют. При этом их содержимое объединяется, а затем внутри клетки образуется сумка — аск — особый орган спороношения, в котором развиваются аскоспоры (обычно по 8 спор в сумке). При благоприятных условиях дрожжи интенсивно размножаются почкованием, а при неблагоприятных гибнут, оставляя весьма устойчивые к воздействию окружающей среды споры. При почковании сбоку дрожжевой клетки вначале появляется бородавочка-почка. Она получает часть ядра и аскоспор от материнской клетки, быстро растёт, отделяется от материнской клетки и начинает жить как самостоятельный грибок. При некоторых условиях дочерняя почка, ещё не отделившись от материнской, образует другие почки, а те, в свою очередь, новые. В результате на поверхности бродильной жидкости возникает гладкая плёнка белого или бежевого цвета из сцепленных между собой грибков — дрожжевая колония. Время достижения дрожжевым грибком половой зрелости зависит от температуры и составляет [7]:

При температурах ниже 5оС и выше 50оС дрожжевые грибки утрачивают свою сбраживающую способность, а при 70о полностью погибают, на чём основан процесс пастеризации — консервирования пищевых продуктов путём нагревания до 70оС в течение 15–30 мин. При этом неспороносные бактерии погибают, но полного освобождения пищи от живых микроорганизмов — стерилизации не происходит, т.к. споры такое нагревание выдерживают. Оптимальной температурой для развития сахаромицетов является температура 30–37оС, а для сбраживания ими виноградного сока в вино — 15–18оС, т.к. при этой температуре образуется меньше упомянутых выше сивушных масел.
Слишком высокая концентрация сахара в сбраживаемой жидкости (как внесённого, так и содержащегося в самих ягодах винограда) вредно влияет на дрожжевые грибки: уже при 15% брожение замедляется или может остановиться совсем.
Получающийся при брожении спирт тоже замедляет рост грибков. При концентрации спирта 5 об.% дрожжи перестают размножаться, а при 12–15 об.% практически полностью прекращают спиртовое брожение. Отдельные виды — расы дрожжей в особенности культурные расы, выращенные на чистых, предварительно очищенных от других микроорганизмов культурах, способны вырабатывать спирт крепостью до 20 об.%, но дикие дрожжи, находящиеся на поверхности сладких ягод и плодов, набраживают не более 10–12% спирта. Однако при удалении спирта из бродильной жидкости или переносе дрожжей в новую, не содержащую спирта жидкость, брожение при наличии соответствующих условий возобновляется вновь. На этом, в частности, основан процесс непрерывного сбраживания в промышленном производстве вина, когда дрожжевая разводка закладывается один раз в начале сезона виноделия [19].
Число известных культур дрожжей очень велико. Существуют культуры, растущие на поверхности бродящей жидкости (дрожжи верхнего брожения), и культуры, собирающиеся на дне сосудов, в которых проводится брожение (дрожжи нижнего брожения). Дрожжи верхнего брожения причиняют массу неудобств виноделу, т.к. под действием углекислого газа образуют на поверхности бродящей жидкости шапку пены, которая при интенсивных первых этапах брожения забивает газоотводящие трубки и водяные затворы. Развивающегося при этом давления углекислого газа достаточно для взрывного разрушения стандартной 20-ти литровой стеклянной бутыли, в чём автор убедился на собственном опыте.
Свои разнообразные энергетические потребности, в том числе в тепле, дрожжевые грибки удовлетворяют за счёт расщепления сахаристых веществ, но как было отмечено выше, конечные продукты этого расщепления зависят от наличия кислорода. При аэробных условиях, т.е. в присутствии кислорода, дрожжи расщепляют сахара полностью до воды и углекислого газа точно также, как это происходит в организме животных и человека. При отсутствии кислорода, т.е. в анаэробных условиях, дрожжи не доводят расщепление до конца, а только превращают сахар в выделяющиеся наружу через стенку клетки спирт и углекислый газ. При этом из одной молекулы сахара освобождается энергии примерно в 20 раз меньше, чем при аэробном процессе. Чтобы компенсировать недостаток энергии дрожжи вызывают усиленное брожение. Тем более, что сбраживающая сила находящегося в дрожжевых грибках фермента такова, что одна его весовая часть в состоянии расщепить от 1 000 до 100 000 весовых частей сахаристого вещества [18].
Помимо тепла дрожжи, как было отмечено выше, нуждаются и в пище, которой им служат соединения калия, магния, производные фосфорной кислоты и, в первую очередь, азотистые соединения, которые нужны для образования белкового вещества самих грибков. Кроме того, для нормального развития дрожжей необходимы очень незначительные количества витаминов группы В. Поэтому в бродящую жидкость полезно добавлять небольшие количества сернокислого аммония или нашатырного спирта (1мл. на 10 л) и слегка подсушенного ржаного хлеба.
Кроме способности вызывать спиртовое брожение, дрожжи полезны ещё и тем, что содержат высококачественный белок, углеводы и богаты витаминами группы В. Жидкие пивные дрожжи улучшают секрецию желудочных желёз и поджелудочной железы, усиливают всасывание пищевых веществ в кишечнике, повышают сопротивляемость организма к инфекциям. Их назначают для приёма внутрь при анемиях, сахарном диабете, фурункулёзе, язвенной болезни и др., а также при необходимости повысить содержание белков в пищевом рационе. Однако среди дрожжей встречаются и патогенные формы, вызывающие заболевания у человека и животных — бластомикозы и кандидамикозы [16].
Углеводы
Вещества, в конечном итоге расщепляющиеся под действием дрожжей на этиловый спирт и углекислый газ, называются углеводами. Это название было введено в литературу в 1884 г. К. Шмидтом [17] на основании мнения, высказанного ещё в 1827 г. биохимиком Г. Пру, согласно которому различные виды сахара, а также крахмал и целлюлоза должны рассматриваться по своему строению как соединения углерода с водой (отсюда и название):
(С + Н2О) n
Это старое название целой группы органических веществ, входящих в состав всех растений и живых организмов, сохранилось, хотя уже давно установлено, что такой формальный взгляд по существу неправилен и что к классу углеводов принадлежат и такие соединения, которые не отвечают указанной формуле.
Углеводы и их превращения известны с древнейших времён, т.к. они лежат в основе процессов брожения, обработки древесины, изготовления бумаги и тканей из растительных волокон. Чрезвычайно важна и многообразна роль углеводов в животном и растительном мире. В растениях они запасаются в виде нерастворимого в воде крахмала, а в животных в виде животного крахмала — гликогена и служат энергетическим резервом для жизнедеятельности.
Все углеводы условно делятся на группы:
Моносахариды или простые сахара.
Олигосахариды, содержащие в молекуле несколько — от 2 до 10 звеньев моносахаридов (дисахариды, трисахариды и т.д.).
Полисахариды — сложные сахара, содержащие много (до тысяч) моносахаридных звеньев.
Олиго- и полисахариды, присоединяя при определённых условиях воду, расщепляются (гидролизуются) на молекулы моносахаридов или более простых полисахаридов. Моносахариды, за исключением глюкозы и фруктозы, в свободном виде встречаются в природе крайне редко. Значительно более широко распространены олигосахариды — например сахароза (бытовое название сахар), и полисахариды, к числу которых относятся крахмал, инулин и целлюлоза (клетчатка). Сахарозу ещё называют дисахаридом, потому что, присоединяя при гидролизе одну молекулу воды, она распадается на две молекулы — глюкозу и фруктозу.
Глюкоза — моносахарид — виноградный сахар, представляет собой белое сладкое кристаллическое вещество, хорошо растворимое в воде. Первые наблюдения над виноградным сахаром были сделаны в XVII веке немецким химиком и врачом И. Глаубером, сообщившим о его получении из соков различных плодов, а также изюма и мёда. Глюкоза значительно менее сладкая, чем сахароза и вместе с фруктозой составляет главную часть пчелиного мёда.
Фруктоза — моносахарид — фруктовый или плодовый сахар, представляет собой бесцветные, сладкие на вкус кристаллы, хорошо растворимые в воде. Фруктоза слаще глюкозы в три раза и представляет собой ценный пищевой продукт, хорошо усваиваемый организмом. В пчелином мёде содержится 50% фруктозы.
Фруктоза и глюкоза являются изомерами, т.е. химическими соединениями одинаковыми по составу и молекулярной массе, но различающимися по строению и, как следствие, по физическим и химическим свойствам. По этой причине формула обоих веществ одинакова — С6Н12О6.
При спиртовом брожении вещество состава С6Н12О6 под действием упомянутого выше фермента дрожжей зимазы разлагается на спирт С2Н5ОН и углекислый газ СО2. При этом выделяется некоторое количество тепловой энергии — 690 ккал ∕моль [25], т.е.
.

Эта энергия частью расходуется на поддержание температуры тела дрожжевого грибка, но и не только для этого, т. к. биологические системы должны запасать энергию в каком-то виде так, чтобы впоследствии использовать её в химических реакциях для обеспечения своей жизнедеятельности. Например, как было отмечено выше, энергия необходима дрожжевому грибку для синтеза белка из его составных частей — аминокислот.
Сахароза (в быту сахар) — дисахарид — тростниковый или свекловичный сахар, представляет собой белые сладкие на вкус кристаллы, хорошо растворимые в воде. В сахарном тростнике содержится 14—16% сахара, в клубнях сахарной свёклы — 16—20%, а в некоторых сортах до 27%.
Сахар впервые начали выделывать свыше 2500 лет назад. Ещё раньше в Индии умели разводить сахарный тростник и его сладкий сок употребляли в пищу. Позднее из этого сока стали получать выпариванием твёрдый сахар-сырец коричневого цвета. Твёрдый сахар белого цвета впервые научились получать в Иране. Для этой цели сок сахарного тростника сгущали нагреванием в котлах, подливая к нему молоко. При этом красящие примеси уходили в пену. От иранцев искусство делать белый сахар перешло в Египет. Тысячу лет тому назад египетский сахар завозили в Европу и продавали в аптеках как лекарственное средство. В XVI веке сахарный тростник стали разводить в Америке на острове Куба и в Мексике. Долгое время в Америке производили только тростниковый сахар-сырец и привозили его в приморские города Европы, где он очищался на рафинадных заводах. В России первый сахарно-рафинадный завод, перерабатывающий привозной тростниковый сахар, был построен в Петербурге в 1719 г.
В середине XVIII века было выяснено, что в свёкле и многих других растениях, произрастающих в самой Европе, тоже находится сахар, причём в количествах, достаточных для промышленного производства.
Первый завод в Европе по производству сахара из свёклы был построен в Германии в 1799 г. Однако это производство вскоре заглохло и возродилось вновь только в двадцатых годах XIX века. В России первый завод по производству свекловичного сахара был построен в 1802 г в Тульской губернии, а в 1805 г. в России было добыто из сахарной свёклы всего 5 тонн сахара [18], поскольку себестоимость продукта была крайне велика — фунт сахара стоил 2 руб, а корова — 5 руб. Однако по мере усовершенствования технологии цена непрерывно снижалась и упала до 14 коп. за фунт. По объёму производства сахара Россия накануне Первой мировой войны занимала 2-ое место в мире после Германии.
При попадании сахара (сахарозы) в организм человека или при внесении сахара в бродильную жидкость, содержащую дрожжи, он под действием фермента дрожжей инвертазы присоединяет молекулу воды и распадается на глюкозу и фруктозу:
,
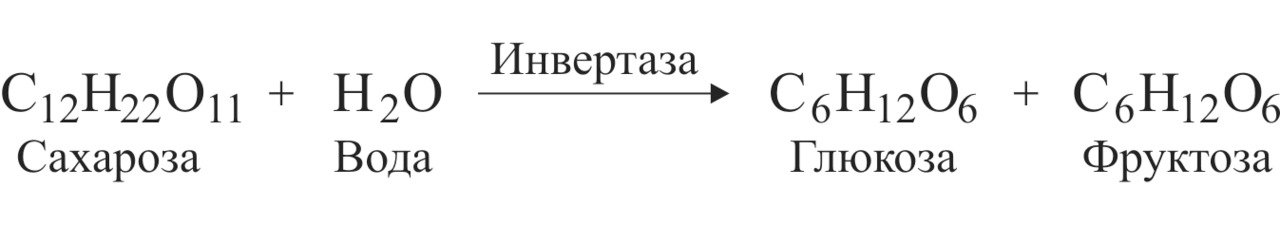
которые, в свою очередь, распадаются на спирт и углекислый газ как было описано выше. В течение дня организм здорового и непьющего человека способен синтезировать из пищи от 1 до 9 г этилового спирта [4] и ферментных мощностей организма вполне хватает для его окисления с целью получения энергии. При больших дозах введённого в организм алкоголя ферменты не успевают его окислять. В организме накапливается этиловый спирт и продукт его частичного распада — ядовитый ацетальдегид, что вызывает симптомы обширной интоксикации, называемой в быту похмельем. Считается, что ежедневная доза спиртного, эквивалентная 20 г чистого алкоголя, относительно безопасна для здоровья. Но важна не только доза выпитого алкоголя, но и время его употребления. Тот, кто следит за своим здоровьем, по опыту знает, что не стоит принимать спиртное ранее трёх часов дня и после полуночи.
Крахмал — полисахарид, состоит из смеси двух других, менее сложных полисахаридов — амилозы (30%) и амилопектина (70%). Представляет собой белый порошок нерастворимый в воде и является важнейшим резервным углеводом всех растений. В природе крахмал вырабатывается растениями и находится у них в клетках в виде зёрен, форма и величина которых в различных растениях разная. Например, клубни картофеля содержат 20% крахмала при содержании воды 75%, а в зёрнах пшеницы до 70% крахмала.
При нагревании с водой зёрна крахмала разбухают и образуют клейстер. При частичном гидролизе крахмала или при нагревании его до температуры 180–200оС крахмал расщепляется на декстрины — твёрдые, но уже растворимые в воде вещества, состоящие из более простых углеводов. По молекулярной массе декстрины занимают промежуточное положение между молекулярными массами глюкозы и крахмала. Блеск накрахмаленной рубашки, появляющийся при её глажении, обусловлен декстринами, образующимися в результате разрушения крахмала горячим утюгом. Блестящая корочка свежеиспечённого хлеба также состоит из декстринов.
Под влиянием широко распространённого в растительном мире фермента диастазы крахмал гидролизуется, присоединяя воду, и образует дисахарид мальтозу или солодовый сахар:

В технике этот процесс называют осахариванием крахмала, независимо от того из чего он получен — картофеля, свёклы, кукурузы или злаковых культур.
В связи с этим, полезно иметь представление о технике получения этилового спирта из крахмала, содержащегося, например, в картофеле [18]. Клубни картофеля предварительно моют, распаривают под давлением 3–3,5 атм. в конических железных котлах, а затем выдувают через находящуюся снизу котла выдувную трубу. При этом принимают меры для охлаждения, поскольку температуры выше 65оС уничтожают диастазу. Из-за резкого уменьшения давления на выходе из котла оболочки клеток картофеля разрываются, содержащиеся в них зёрна крахмала освобождаются, и образуется вязкая киселеобразная субстанция — клейстер, аналогичный клейстеру из пшеничной или ржаной муки. После добавления к нему солода происходит гидролизация крахмала по приведённой выше формуле. По окончании этого процесса первоначально густая жидкость становится подвижной, более прозрачной и сладкой на вкус. Её охлаждают до 18–20оС и подвергают спиртовому брожению путём добавления винных дрожжей.
Первые несколько часов выделения спирта почти не происходит — дрожжи интенсивно размножаются, используя находящийся в бродильной жидкости кислород. Примерно через 10 часов их количество увеличивается в 10–14 раз, кислород в бродильном сосуде истощается и начинается процесс интенсивного брожения с выделением тепла. В ходе этого процесса содержащийся в дрожжевых грибках фермент мальтаза расщепляет солодовый сахар мальтозу до виноградного — глюкозы, а другой фермент дрожжей зимаза расщепляет глюкозу до этилового спирта и углекислого газа, как это было описано выше, т.е.:
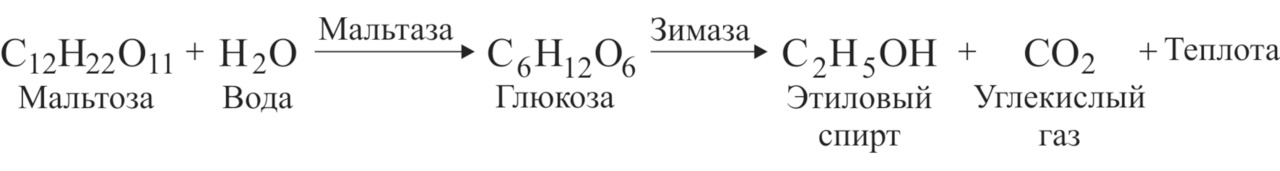
На самом деле формулы спиртового брожения выглядят гораздо сложнее, их запись занимает почти целую книжную страницу [5], но в приведённом упрощённом виде они вполне достаточны для понимания сути происходящих процессов.
Для полноты картины следует упомянуть ещё один углевод, расщепляющийся под действием дрожжей на спирт и углекислый газ. Это весьма полезный в быту дисахарид — лактоза или молочный сахар, открытый в 1612 г. Бартолетти и названный им манна, т.к. одно время он считался эффективным лечебным средством [8]. Молочный сахар состоит из остатков моносахаридов — глюкозы и галактозы и присутствует в молоке всех млекопитающих. При определённых условиях он сначала гидролизуется под действием фермента ß-галактозиазы в моносахариды, а затем сбраживается в кисломолочные продукты, содержащие незначительные количества спирта. Наиболее известными из них являются кумыс — шипучий пенящийся напиток со спиртовым вкусом и запахом из кобыльего (реже коровьего и верблюжьего) молока с содержанием спирта от 1 до 3%, а также обыкновенный кефир с 0,16–1,22% спирта [17]. При таком содержании спирта в кефире его, как заметил премьер министр РФ В. Путин 13.02.2011 г., «нужно выпить тазик», чтобы не пройти водительский тест на алкоголь.
Инулин — полисахарид — содержится в корнях тапинамбура (земляной груши), корнях цикория и др. Представляет собой белый порошок или прозрачные кристаллы. Не растворим в холодной воде. Дрожжи не сбраживают инулин, ферменты солода его не осахаривают. В водной среде при 55–60оС инулин превращается в сбраживаемые сахара под действием находящегося в нём самом фермента инулазы. В 30-е годы прошлого века в СССР была разработана технология получения этилового спирта как из инулина, так и из цикория [27].
Целлюлоза (клетчатка) — полисахарид — представляет собой вещество белого цвета, нерастворимое ни в воде, ни в спирте. Она является главной составляющей частью клеточных стенок растений (отсюда название) и обеспечивает прочность и эластичность растительных тканей. В отличие от других природных полисахаридов, являющихся для растений резервными веществами, которые растения могут преобразовать для своих потребностей в другие вещества, целлюлоза не может быть снова расщеплена в их организме или использована растением каким-либо другим способом.
По своему количеству целлюлоза занимает первое место в мире среди всех остальных природных органических соединений. Гигроскопическая вата, белые хлопчатобумажные и льняные ткани, хорошие сорта фильтровальной бумаги состоят главным образом из целлюлозы (клетчатки). Наиболее чистая природная клетчатка содержится в волосах семян хлопчатника, в которых она составляет 80–90% (при 6–8% воды). Древесина деревьев хвойных пород содержит около 50% клетчатки, лиственных — значительно меньше. Впрочем, чистая целлюлоза находится лишь в молодых клетках растений; по мере старения клеток в них отлагается инкрустирующие вещества, в особенности лигнин — аморфное вещество жёлто-коричневого цвета, вызывающее одревеснение и увеличение прочности растительных клеток.
В организме человека не вырабатывается достаточного количества ферментов (мальтазы и амилазы) для расщепления целлюлозы до усваиваемой глюкозы — иначе мы не ограничивались бы грушами, а получали удовольствие, откусывая прямо от ствола. Но у травоядных животных есть фермент целлюлаза, вырабатываемый микрофлорой кишечника, под действием которой целлюлоза расщепляется до глюкозы.
В технике более или менее чистую целлюлозу получают в громадных количествах при производстве бумаги.
В контексте данной книги имеет смысл рассмотреть процесс производства из целлюлозы гидролизного этилового спирта, поскольку его часто используют для фальсификации водки вместе с рассмотренным выше синтетическим этиловым спиртом, вырабатываемым из этилена.
Для производства этилового спирта из целлюлозы древесные опилки и другие отходы лесоперерабатывающей промышленности нагревают под давлением с 0,1% раствором серной кислоты. В результате такой обработки целлюлоза расщепляется до глюкозы и образуется сладкий сироп. Этот сироп сбраживают, используя винные дрожжи, и перегоняют в спирт, который по способу производства называют гидролизным спиртом. Он содержит заметное количество вредного для организма метилового спирта и предназначен для использования в технических целях, в частности, для получения синтетического каучука. В среднем из 1 тонны сухого древесного сырья, в том числе вылущенных кукурузных початков, лузги семян подсолнечника, древесных опилок и т. п. можно получить 175 литров этилового спирта. Такое же количество спирта можно выработать из 0,6 тонны зерна или 1,6 тонны картофеля [19]. Хорошим сырьём для производства этилового спирта служат даже корневища злостного сорняка — пырея [27].
В заключение стоит упомянуть об одном слове, давно утратившим свой первоначальный смысл, но имеющим непосредственное отношение к рассматриваемой теме. В обиходе иногда говорят буза, подразумевая под этим что-то простенькое и никчёмное. На самом деле буза — это спиртовой напиток наподобие пива, но без хмеля, который раньше вырабатывали в Крыму и на Кавказе из проса, содержащий 4—6% спирта [5].
И последнее. Как известно пиво тоже представляет собой продукт спиртового брожения. Для его производства нужны ячмень, солод, хмель, вода и пивные дрожжи. Солод превращает крахмал ячменя в солодовый сахар, пивные дрожжи сбраживают его в спиртосодержащий напиток, а хмель придаёт пиву специфический вкус и аромат. Содержание этилового спирта в приготовленном таким способом пиве не превышает 3,5–3,7% об. (только в три раза больше, чем у упомянутого выше кефира!). Поэтому пиво всегда было напитком для утоления жажды, а не для опьянения. Однако в последнее время производители пива стали добавлять в сусло ингредиенты, повышающие при спиртовом брожении содержание в пиве спирта, например, рисовую муку, отходы сахарного производства — мелассу и пр. Такой напиток, строго говоря, нельзя называть пивом. Он стал пьянящим, с тяжёлым похмельем, а при регулярном и длительном употреблении наносящим вред здоровью (вплоть до опухоли поджелудочной железы и рака прямой кишки при регулярном употреблении 0,5 литра в день [4]). Термин «пивной алкоголизм» в ходу у медиков уже лет двадцать. Всё дело в том, что, повышая содержание спирта в пиве путём выбраживания дополнительного количества крахмала, например, крахмала той же рисовой муки, производители тем самым увеличивают и содержание в пиве сивушных масел. Все сивушные масла — высшие спирты — являются наркотиками с наркотическим действием значительно большим, чем у этилового спирта. Но если при производстве этилового спирта из крахмалосодержащего сырья сивушные масла можно отделить перегонкой или очисткой водки на активированном угле, то из пива их удалить невозможно. Они поступают в организм, вызывая сначала привыкание, а затем и алкогольную зависимость.
Из содержания данной главы следует, что использование виноградного сырья для производства этилового спирта в домашних условиях обладает рядом преимуществ по сравнению с его получением из крахмалосодержащего сырья. К числу таких преимуществ относятся:
— простота подготовки сырья и его сбраживание, практически не требующее применения дрожжей и минеральной подкормки,
— минимальное количество терпимо, чтобы не сказать приятно, пахнущих отходов и, как следствие, простота их утилизации (например, компостирование виноградного жома в дачном хозяйстве),
— незначительное содержание в отгоне сивушных масел из-за отсутствия в сусле посторонних белковых веществ,
— возможность увеличения выхода спирта путём простого добавления в сусло сахара в количествах, не угнетающих брожение,
— наконец, минимальная себестоимость по сравнению с крахмалосодержащим сырьём, т.к. все затраты приходятся только на сбор и транспортировку винограда с дачного участка, а трудоёмкость выращивания винограда весьма незначительна.
Прежде, чем перейти к рассмотрению вопросов, связанных непосредственно с перегонкой спиртосодержащих жидкостей, имеет смысл ознакомиться с особенностями физических процессов кипения и испарения жидкости, и конденсации её паров, которые протекают в перегонном аппарате любой конструкции.
Глава 4. Испарение, кипение, конденсация
Испарение — представляет собой процесс перехода вещества из жидкого состояния в газообразное, т.е. в пар. Испарение происходит за счёт того, что постоянно находящиеся в тепловом движении молекулы жидкости в результате соударений с другими движущимися молекулами случайно получают энергию, достаточную для преодоления сил сцепления с жидкостью и покидают её со свободной поверхности. Поэтому испарение возможно при любой температуре, но с возрастанием температуры возрастает интенсивность теплового движения молекул и скорость испарения увеличивается. При переходе в пар молекула должна преодолеть не только силы сцепления с другими молекулами в жидкости, но и совершить работу против молекул уже образовавшегося пара, которые путём таких же случайных соударений могут вернуть её обратно в жидкость. Поскольку обе эти работы совершаются за счёт кинетической энергии молекулы, то в результате испарения жидкость охлаждается. Поэтому, чтобы процесс испарения проходил при постоянной температуре, жидкости необходимо постоянно сообщать некоторое количество теплоты. При процессе обратном испарению — конденсации, т.е. при образовании жидкости из пара, происходит выделение теплоты, и если её не отводить, конденсация прекратится. Примером этому служит паровозный гудок — проходящий через него перегретый пар из котла разогревает корпус гудка и пар, не успевая конденсироваться, вырывается наружу. В результате гудок гудит, а не булькает, разбрасывая брызги.
В закрытом сосуде при заданной постоянной температуре испарение будет происходить до тех пор, пока всё пространство над оставшимся избытком жидкости не будет заполнено её насыщенным паром. Между жидкостью и её насыщенным паром существует динамическое равновесие: число молекул, покидающих жидкость в единицу времени, равно числу молекул пара, возвращающихся за это же время в жидкость. Для жидкостей одного состава каждой температуре соответствует строго определённое давление её насыщенного пара. Отображённые в графическом виде эти зависимости носят название кривые равновесия и являются важнейшими характеристиками состояния вещества. Позднее они понадобятся при рассмотрении процессов дистилляции и ректификации.
Кипением называют процесс испарения жидкости не только с её свободной поверхности, но и по всему объёму внутрь образующихся в ней пузырьков пара [29]. За счёт интенсивного испарения пара внутрь пузырьков они растут, всплывают на поверхность и содержащийся в них насыщенный пар переходит в паровую фазу над жидкостью. Спокойное испарение жидкости переходит в кипение тогда, когда давление насыщенного пара внутри пузырьков в жидкости начинает превышать внешнее атмосферное давление на жидкость. Температура, при которой происходит кипение жидкости, находящейся под постоянным давлением, называется температурой кипения. Температуру, при которой жидкость кипит при атмосферном давлении 760 мм рт. ст., принято называть нормальной температурой кипения. Она является важнейшим параметром чистого вещества в жидком виде.
Если пар кипящей жидкости свободно выходит на воздух, то её температура остаётся постоянной. При этом всё количество подводимого тепла уходит на парообразование, а интенсивность кипения определяется скоростью подачи тепла. При увеличении внешнего давления температура кипения жидкости увеличивается, при уменьшении — понижается, вплоть до того, что если интенсивно откачивать образующиеся пары, то жидкость закипит даже при комнатной температуре. Этим явлением пользуются при перегонке жидкостей, разлагающихся при высокой температуре [31].
Для поддержания кипения к жидкости необходимо постоянно подводить теплоту, которая расходуется на парообразование, вследствие чего кипение неразрывно связано с теплообменом, при котором теплота постоянно передаётся от поверхности нагрева к жидкости. Поскольку скорость теплообмена имеет конечное значение и не так уж велика, в кипящей жидкости устанавливается определённое распределение температуры: у поверхности нагрева, т.е. на дне перегонного сосуда, жидкость несколько перегрета относительно температуры кипения. Величина перегрева зависит как от физико-химических свойств самой жидкости, так и от качества граничащих с ней твёрдых поверхностей. Тщательно очищенные от растворённых газов жидкости при соблюдении особых мер предосторожности можно перегреть в сосудах из гладкого кварцевого стекла на десятки градусов без закипания. Но если такая перегретая жидкость, в конце концов, закипает, то процесс кипения протекает настолько бурно, что напоминает взрыв. Вскипание сопровождается расплёскиванием жидкости и гидравлическими ударами, которые могут вызвать разрушение сосудов. Так как теплота перегрева расходуется на парообразование, то жидкость быстро охлаждается до температуры насыщенного пара. На практике такое поведение перегретой жидкости называют толчками. При перегонке жидкости с целью разделения на отдельные фракции они, кроме опасности разрушения аппаратуры, нежелательны ещё и тем, что могут забросить жидкие продукты из куба прямо в холодильник, сведя на нет результаты перегонки.
Перегрев объясняется тем, что для образования первоначальных зародышей для парообразования — микроскопических пузырьков газа необходимо преодолеть силы взаимного сцепления молекул внутри жидкости. Однако, при наличии так называемых центров кипения — пузырьков, образующихся из растворённых в жидкости газов и газов, адсорбированных в порах, складках и повреждениях стенок сосудов, а также на мельчайших твёрдых взвешенных в жидкости частицах, перегрев не превышает нескольких долей градуса и кипение имеет устойчивый спокойный характер. В обиходе такое кипение, например, воды в чайнике, называют пузырчатым кипением.
С увеличением температуры поверхности нагрева растворённые в жидкости газы начинают интенсивно выделяться, число центров кипения возрастает, всё большее количество образовавшихся пузырьков всплывает на поверхность жидкости, вызывая её интенсивное перемешивание. Это приводит к значительному росту теплового потока от поверхности нагрева к кипящей жидкости. Соответственно возрастает и количество образующегося пара.
При достижении максимального (критического) значения теплового потока начинается второй режим кипения — переходный. При этом режиме значительная доля поверхности нагрева покрывается сухими пятнами из-за расширяющегося взаимного слияния пузырьков пара. Теплоотдача и скорость парообразования в этих местах резко снижаются, т.к. пар обладает меньшей теплопроводностью, чем жидкость. Наступает кризис кипения. Когда же вся поверхность нагрева обволакивается тонкой паровой плёнкой, наступает третий — плёночный режим кипения. При нём теплота от раскалённой поверхности передаётся к жидкости через паровую плёнку путём теплопроводности и излучения. На практике плёночный режим кипения может быть достигнут, когда при дробной перегонке жидкость, уже освобождённая от взвешенных частиц и растворённых газов при предыдущей перегонке, подвергается нагреву вмонтированными в перегонный куб тепло-электронагревателями — ТЕНами с несообразно большой мощностью. В этом случае прогорание стенки ТЕНа не менее опасно, чем прогорание стенки котла паровой турбины.
Наиболее подходящий для реализации поставленной цели пузырчатый режим кипения, исключающий возникновение толков перегоняемой жидкости в нагреваемом сосуде, может быть достигнут несколькими путями. В лабораторной практике, когда для перегонки используется жаропрочная стеклянная колба с шарообразным дном, применяются так называемые кипелки [31]. Они представляют собой очень тонкие стеклянные трубочки наподобие трубочек, используемых в ртутных медицинских термометрах, запаянные с одного конца. Эти трубочки помещаются в колбу под углом к горизонтали открытым концом вниз, чему способствует форма дна колбы. При нагревании жидкости в колбе воздух в трубочках нагревается, расширяется и крошечными пузырьками выходит наружу, образуя центры парообразования. Практическое использование таких кипелок для решения поставленной задачи представляется нецелесообразным, т.к. дно перегонных аппаратов плоское и надёжно установить на нём хрупкие кипелки под некоторым углом, да ещё в условиях бурлящей при кипении жидкости просто невозможно.
Другой способ организации пузырчатого кипения заключается в том, что в куб перегонного аппарата вносятся твёрдые вещества с развитой поверхностью, на которой адсорбированы кислород, азот и другие, содержащиеся в воздухе газы. Выделяющиеся при нагревании микропузырьки этих газов будут служить центрами парообразования. Примером таких веществ являются битые кусочки старой доброй общепитовской тарелки из керамики, исключая её глазурованные участки. Недостаток этого способа состоит в его затратности — кусочки керамики так пропитываются остатками жидкости в перегонном кубе (преимущественно сивушными маслами), что полностью избавиться от неприятного запаха невозможно даже путём прокаливания их на огне.
Наконец, третий способ предотвращения перегрева, связанной с ним задержкой кипения и последующими толчками, состоит в организации перегрева в ограниченном объёме. Для этого на дно перегонного аппарата помещают или неглубокие металлические колпачки с зазубренными краями дном вверх, или диск с выпуклой канавкой — так называемый «сторож» для кипячения молока. В этом случае перегрев жидкости происходит в малом объёме между, поверхностью нагрева и дном колпачка (или выпуклостью в диске). Недостатком применения колпачков является их самопроизвольное опрокидывание в бурлящей жидкости зазубренными краями вверх. Диск-«сторож» трудоёмок в изготовлении, т. к. канавка должна быть отформована на обеих его сторонах, тем более, как будет показано ниже, в этом нет никакой необходимости.
В описанной ниже конструкции перегонного аппарата проблема толков при кипении решена следующим образом. Во-первых, дно и прилегающие к нему вертикальные стенки бака подвергнуты изнутри пескоструйной обработке, которая в домашних условиях может быть с успехом заменена на обработку не очень мелкозернистой шкуркой — достаточно просто затереть до матового состояния гладкую поверхность нержавеющей стали, которая получается после прокатки листа. Такая обработка создаёт на поверхности нагрева микрорельеф, необходимый для увеличения адсорбции газов. Во-вторых, на дно бака помещают 4–5 шт. специальных «кипелок».
Для изготовления «кипелки» из листовой нержавеющей стали толщиной 0,3–0,4 мм. вырезается кружок диаметром 35–40 мм. Кружок помещают на подходящий брусок дерева, желательно из древесины твёрдых пород, и на нём при помощи не очень острого керна набивают три углубления. Они располагаются примерно в 5–7 мм. от края кружка так, чтобы угол между соседними углублениями составлял примерно 120о. Не сдвигая кружок с места, его рихтуют молотком, чтобы восстановить плоскость, а затем замеряют высоту выступа на обратной стороне — вместе с толщиной кружка она должна составлять 1,5–2,0 мм. Затем кружок переворачивают и с обратной стороны накернивают ещё три углубления так, чтобы они были сдвинуты относительно углублений на другой стороне примерно на 60о, и, не сдвигая кружок с места, снова его рихтуют для восстановления плоскости. Изготовленная таким способом «кипелка», представляет собой что-то вроде трёхногого столика с ножками по обеим сторонам столешницы (рис.1).
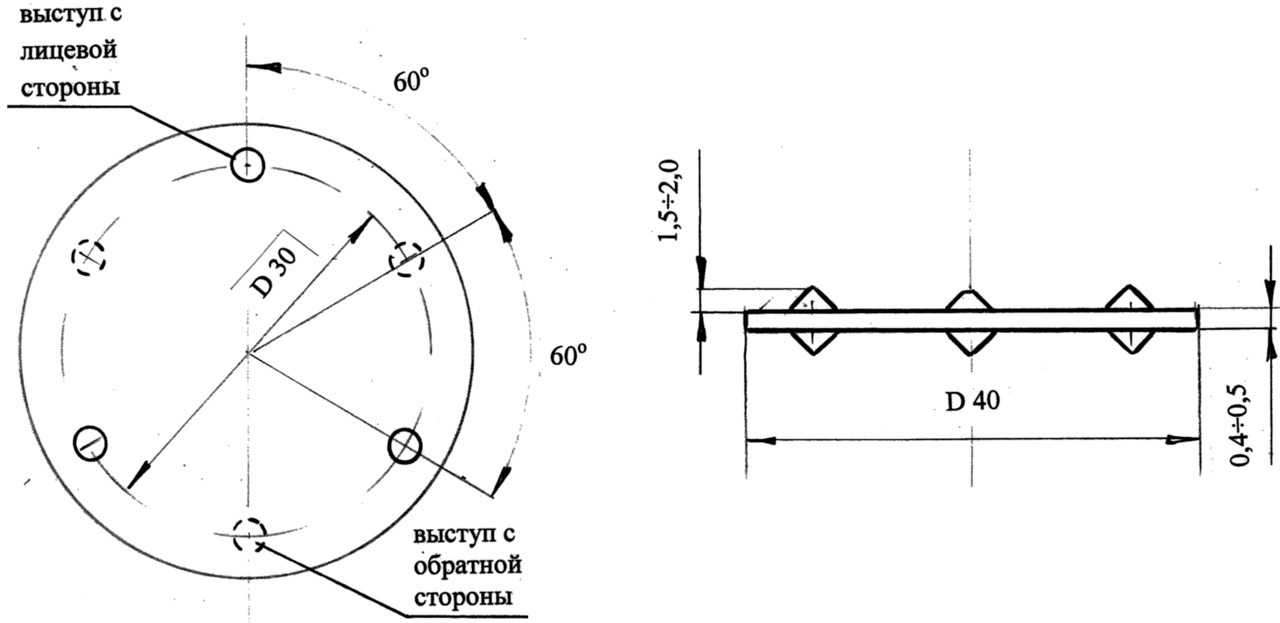
Рис.1. Конструкция «кипелки», используемой для перегонки.
Как бы такую «кипелку» не бросали в бак, она всегда падает на три ножки одной или другой стороной, обеспечивая перегрев жидкости в малом объёме, заключённом между дном перегонного аппарата и нижней поверхностью стоящей на выступах «кипелки». Кроме того, «кипелки» такой конструкции просты в изготовлении, легко моются и занимают незначительную часть площади дна бака, не препятствуя тепловому потоку. При перегонке непрерывное и равномерное позвякивание таких «кипелок» о дно аппарата указывает на то, что режим нагрева выбран правильно. По мере испарения из куба низкокипящего компонента — спирта позвякивание «кипелок» затихает и одновременно уменьшается скорость перегонки. Для её восстановления необходимо несколько увеличить интенсивность нагрева куба. При этом удобно ориентироваться на звук позвякивающих «кипелок».
Если для изготовления «кипелок» использовать достаточно чистую листовую медь (не менее 9999), то «кипелки» одновременно могут выполнить ещё одну функцию — способствовать очистке дистиллята от сернистых соединений [69]. Эти соединения возникают виноматериале в процессе естественного брожения и придают тухлый запах дистилляту после первой перегонки. Если количество сернистых соединений в дистилляте достаточно велико, то медные «кипелки» после второй перегонки покроются тёмным налётом, содержащим серу. Однако в дистилляте, полученном перегонкой виноградного вина или настоя на виноградных выжимках, этот эффект не наблюдается. Более того, диоксид серы часто добавляют в виноградные вина для предотвращения их скисания в количестве от 160 мг/л в красные вина до 400 мг/л в сладкие белые [70]. Но использование нелужёной меди в конструкции дистилляторов имеет и отрицательные стороны, о чём будет сказано в главе 6.
Кроме гидравлических ударов и толчков ещё одним осложнением, возникающим при кипении жидкости, является вспенивание. Поднимающиеся на поверхность жидкости пузырьки пара самопроизвольно лопаются. Однако, при наличии в жидкости (особенно на её поверхности) взвешенных частиц органических соединений и при высоких темпах нагрева пузырьки не успевают лопаться и образуют пену, забивающую перегонный аппарат. Это обстоятельство необходимо учитывать при выборе интенсивности нагрева бака, особенно на первой стадии дробной перегонки, когда перегоняемая жидкость содержит множество органических остатков от брожения.
Есть ещё один специфический момент, который необходимо учитывать при конструировании перегонного аппарата. Он заключается в том, что всплывший на поверхность кипящей жидкости газовый пузырёк лопается с образованием мельчайших капель. Эти капли при подходящих условиях, таких как высокие скорости пара и малое расстояние от поверхности кипящей жидкости, могут увлекаться в выводное устройство и загрязнять отгон продуктами из бака.
Скорость потока пара на входе в холодильник перегонного аппарата можно приблизительно оценить, предположив, что в его кубе кипит чистая вода — такая ситуация имеет место на последних этапах первой перегонки. Исходя из реальной скорости перегонки 15 мл/мин — при больших скоростях в аппарате описанной ниже конструкции происходит интенсивное пенообразование, и плотности воды на выходе из холодильника 0,998 г/мл при 20оС [71], получаем скорость выхода дистиллята в г/мин равную 14,97 г/мин. Такое же количество воды, только в виде насыщенного водяного пара, должно поступать в минуту на вход холодильника. Плотность водяного пара при 100оС составляет 0,598х10—3 г/мл, т.е. на вход холодильника для получения 14,97 г дистиллята должно поступать в минуту 25 литров водяного пара. Это достаточно большая скорость, при которой пар может подхватывать капли кипящей в кубе жидкости и заносить их в холодильник при первой перегонке. Поэтому в аппарате должен быть предусмотрен каплеотражатель.
Ниже будет приведена конструкция эффективного каплеотражателя с кулисой, в которой поток пара дважды меняет направление движения на 180о.
Ознакомившись с протекающими в перегонном аппарате процессами испарения, кипения, вспенивания и каплеобразования, перейдём к другим — дистилляции и ректификации.
Глава 5. Дистилляция и ректификация
Как было отмечено выше, термин дистилляция происходит от латинского слова, означающего буквально «стекание каплями». Однако позднее под ним стали понимать простую перегонку — однократное испарение жидкости, нагреваемой в перегонном сосуде (кубе) и конденсации её паров в холодильнике.
При кипении жидкости одного состава поступающий в холодильник пар имеет тот же состав, что и жидкость в кубе, а при конденсации пара в холодильнике снова получается исходная жидкость. Простую перегонку применяют для очистки жидкости одного состава от растворённых в ней солей и взвешенных твёрдых частиц. Например, при получении дистиллированной воды из водопроводной для кислотного автомобильного аккумулятора или для разбавления выдержанного в дубовой бочке коньячного спирта при производстве коньяка.
Бесплатный фрагмент закончился.
Купите книгу, чтобы продолжить чтение.