
Бесплатный фрагмент - Формулы + уравнения = химия, которую ты понимаешь
Это не учебник. Это спасательный круг — с понятным языком, без занудства и фраз типа «самостоятельно проанализируйте». Здесь шесть коротких, логичных шагов — от «вообще ничего не понимаю» до «эй, я сам могу объяснить это однокласснику!».
Вместе с Еленой Викторовной — не строгой училкой, а нормальным проводником — ты научишься читать формулы, отличать кислоты от солей, уравнивать реакции и понимать, что за чем стоит. Всё чётко, без перегруза — с примерами, подсказками и местами даже с юмором.
Для тех, кто устал пугаться химии.
Для родителей, которые не хотят лезть в свой старый учебник химии.
Для всех, кто хочет сказать: «Ну всё, химия — ты мне больше не страшна».
Мой будущий ученик
Раз ты здесь — значит, в тебе есть желание понять. А это уже начало.
Стоп. А вдруг снова не сработает?
Может, ты уже открывал учебник — и через три минуты откладывал, потому что «ничего не понятно и в голове каша».
Может, химия кажется тебе чем-то сложным, будто она «не для тебя».
Такое чувство знакомо очень многим. И ты точно не один.
Но теперь у тебя есть шанс начать иначе.
Меня зовут Елена Викторовна. Я больше 30 лет помогаю школьникам шаг за шагом разложить химию по полочкам — без перегруза и паники.
Эта книга — твоя проба пера. Она не про то, чтобы выучить всё. Она — про то, чтобы наконец-то начало получаться.
Пусть здесь станет немного легче.
Пусть ты увидишь: «Я могу».
А дальше — ты уже пойдёшь увереннее. Не в одиночку. Со мной.
Готов?
Тогда открывай первую страницу.
Пойдём вместе.
Глава 1. Всё не так сложно — просто начни с начала
«Я пыталась списать формулы у Насти, но поняла, что проще научиться. Они, оказывается, как прозвища: у каждого элемента своё, но логичное»
— Даша Составова, любительница тетрадей с наклейками
Чтобы не блуждать, определим, где ты находишься. Отметь, что тебе уже знакомо.

Посчитай, сколько раз ты выбрал вариант «да»

Это твоя книга — работай с ней в своём темпе!
Глава 2. Что такое химическая формула — и зачем она нужна
«Когда я впервые увидел H₂SO₄, подумал, что это пароль от Wi-Fi. Попробовал ввести — не подключилось.
Зато подключился к химии»
— Бывший «гуманитарий», 8 класс
А теперь по науке!
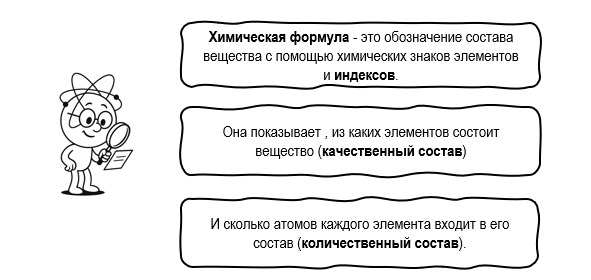
Индексы — это маленькие цифры справа внизу от символа элемента, которые показывают количество атомов данного элемента в молекуле. Если индекс равен 1, то его не пишут.
Коэффициенты — это цифры-множители перед формулой вещества, которые показывают количество молекул.
Примеры:
Углекислый газ, CO₂:
Качественный состав: углерод (C) и кислород (O).
Количественный состав: 1 атом углерода и 2 атома кислорода.
Формула 3H₂SO₄ показывает:
Качественный состав: водород (H), сера (S) и кислород (O)
Количественный состав трёх молекул серной кислоты: 6 атомов водорода, 3 атома серы и 12 атомов кислорода
Виды химических формул
Простейшие формулы показывают только качественный и количественный состав вещества и соотношение между атомами элементов.
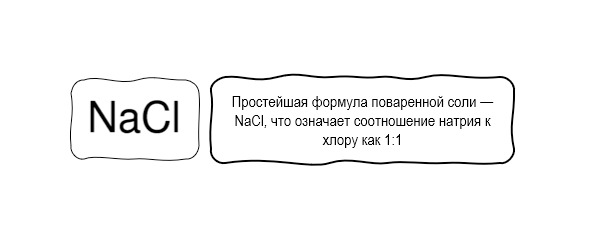
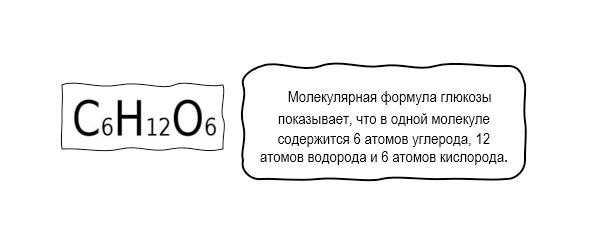
Молекулярные (истинные) формулы показывают точное число атомов химических элементов, входящих в состав одной молекулы вещества.
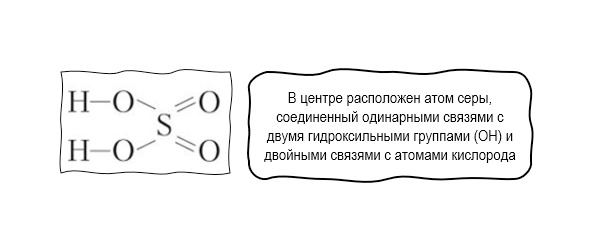
Структурные формулы в графическом виде показывают взаимное расположение атомов в молекуле. Химические связи между атомами обозначаются линиями (чёрточками).
Валентность: первая встреча
Не бойся слова «валентность» — это не заклинание волшебника. Это способ спросить: «Сколько связей может держать атом?»
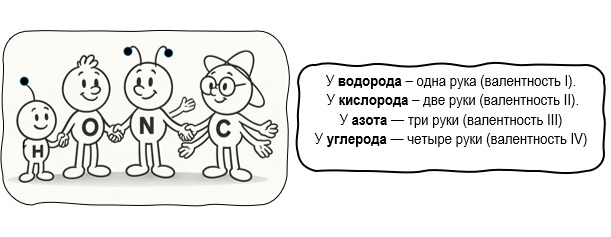
Представь, что атомы — это люди, которые могут держаться за руки. У кого-то — две руки, у кого-то — одна, у кого-то — целых четыре.
Валентность — это сколько «рук» у атома, чтобы соединяться с другими атомами.
Просто запомни идею: валентность = число связей.
Большая практика
1. Визуальные карточки с формулами, валентностью и структурой
Формула: H₂O
⁑ Название: вода
⁑ Состав: 2 атома водорода (H), 1 атом кислорода (O)
⁑ Где встречается: вода, пар, лёд, наш организм
⁑ Валентность элементов: H (I), O (II)
⁑ Структура: H — O—H
Формула: CO₂
⁑ Название: углекислый газ
⁑ Состав: 1 атом углерода (C), 2 атома кислорода (O)
⁑ Где встречается: в выдыхаемом воздухе, газировке
⁑ Валентность элементов: C (IV), O (II)
⁑ Структура: O=C=O
Дальше попробуй выполнить самостоятельно. В случае затруднений, пользуйся различными источниками информации.
Формула: NH₃
⁑ Название:
⁑ Состав:
⁑ Где встречается:
⁑ Валентность элементов:
⁑ Структура:
Формула: CH₄
⁑ Название:
⁑ Состав:
⁑ Где встречается:
⁑ Валентность элементов:
⁑ Структура:
Формула: H₂SO₄
⁑ Название:
⁑ Состав:
⁑ Где встречается:
⁑ Валентность элементов:
⁑ Структура:
2. Кислород в действии
Составь формулы оксидов (веществ, состоящих из кислорода и одного другого элемента).
Используй степени окисления: кислород всегда −2.
а) Cl⁺⁵, As⁺³, Pb⁺⁴, B⁺³
б) Sr⁺², Cu⁺, Mn⁺⁷, Cr⁺⁶
в) Sb⁺⁵, Sn⁺⁴, Hg⁺, Al⁺³
Пример:
Cl⁺⁵ и O⁻² → Cl₂O₅ (наименьшее общее кратное — 10)
3. С водородом — не всё просто
Составь формулы веществ, в которых участвует водород.
Водород может быть как с положительной, так и с отрицательной степенью окисления.
а) C⁻⁴, Na⁺, P⁻³
б) S²⁻, Ca²⁺, I⁻
Подсказка:
Если водород со степенью +1 — он образует соединения с неметаллами с отрицательной степенью окисления.
Если водород в степени −1 — это гидриды активных металлов.
4. Проверь на внимательность: ошибки в степенях окисления
В каждом из приведённых соединений допущена ошибка в степени окисления одного (или нескольких) элементов.
Твоя задача — найти ошибку и исправить:
— Запиши правильные степени окисления для всех элементов
— Объясни, в чём была ошибка
— Запиши верный вариант
S⁺⁶O₃⁻²
N⁻²H₃⁺
S⁺⁶O₂⁻²
K₂⁺C⁺³O₃⁻²
Al⁺²Cl₃
Ca⁺C⁺⁵O₃⁻
Na₂⁺N⁺⁶O₃⁻²
Mg₃⁺³N₂⁻²
Подсказка:
У кислорода почти всегда −2
Водород с неметаллами — +1, с металлами — −1
Индекс — это количество атомов, а не степень окисления!
В соединении сумма всех степеней окисления = 0
5. Проверь формулы: ошибки в составе соединений
Перед тобой — список химических формул. Некоторые из них записаны неверно: нарушен заряд ионов, индексы не соответствуют степеням окисления, формула невозможна.
Твоя задача:
Бесплатный фрагмент закончился.
Купите книгу, чтобы продолжить чтение.